生物强化MFC去除制药废水中的苯酚
)是以微生物为催化剂,将有机物中的化学能转化为电能的生物电化学混合系统,具有原料来源广、清洁环保等优点。在系统完整的生物电化学过程中,有机底物(电子供体)在微生物代谢过程中氧化降解,产生电子和质子,电子首先经呼吸链传递到细胞膜,再由胞外电子转移机制转移到阳极,最终通过外电路传递到阴极,质子通过交换膜传递到阴极室,电子、质子与电子受体(
制药废水具有成分复杂、有机物含量高、可生化性差等特点,属于难处理的工业废水,化学、物理等传统处理方法难以顺应当今绿色、低碳的发展趋势。利用生物法处理制药废水具有经济高效、不产生二次污染的优点。HongyiZHU等构建双室MFC同步处理含恩诺沙星、Cu和Zn的合成废水,该MFC的最大功率密度为(244.2±20.3)mW/m2,恩诺沙星降解率为(67.6±7.1)%,COD去除率为(87.3±1.5)%。严伟富等通过构建序批式双室MFC处理10mg/L的氧四环素人工废水,氧四环素的最高去除率可达99.0%,MFC的最大输出电压为0.55V左右。可见,通过MFC等生物电化学系统处理制药废水具有将废水中蕴藏的能源以电能形式输出的潜力,对污废水净化与能源回收具有重要意义。
生物强化技术通过向污泥、废水等微生物群落中加入功能性菌株,改善原有系统的效能。生物强化技术应用于污水处理系统的优点:1)优化微生物群落结构;2)改善难降解污染物的降解效果;3)提高系统应对多变冲击负荷的能力。如何引入功能性菌株,并使其在系统中有效定殖是生物强化技术的关键步骤。吴恒等利用污泥挂膜和菌剂挂膜方式处理畜禽养殖废水,不同生物强化方式形成的生物膜存在差异,菌剂挂膜方式明显缩短了系统的启动时间,加大了对COD、NH4+-N、TN的去除率。李婷等在焦化废水A2O工艺中采用生物强化技术,添加高效降解菌红球菌后,COD、喹啉、吡啶的去除率明显增加,系统内有机污染物降解菌成为优势菌。
本研究以活性污泥为阳极底物,模拟苯酚制药废水为阳极基质,构建双室MFC系统,添加电活性微生物S.oneidensisMR-1对MFC系统进行生物强化,通过向系统直接加入菌悬液(游离细胞)与固定细胞,对比分析功能性菌株投加形式对混合MFC系统产电性能、污染物去除效果、微生物菌群结构的影响。

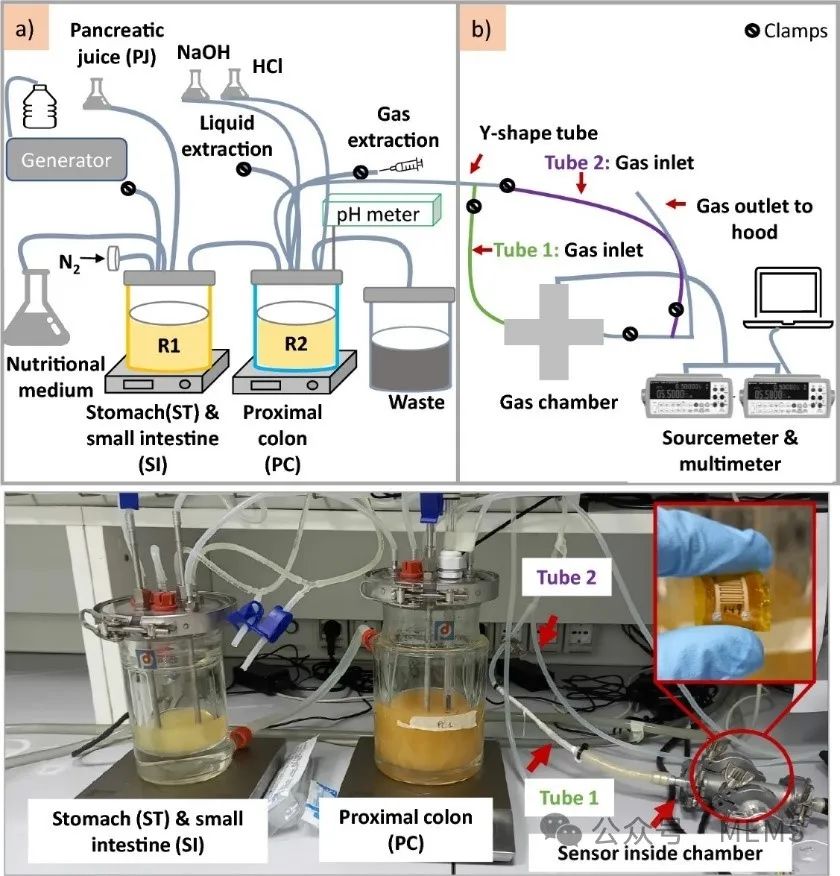
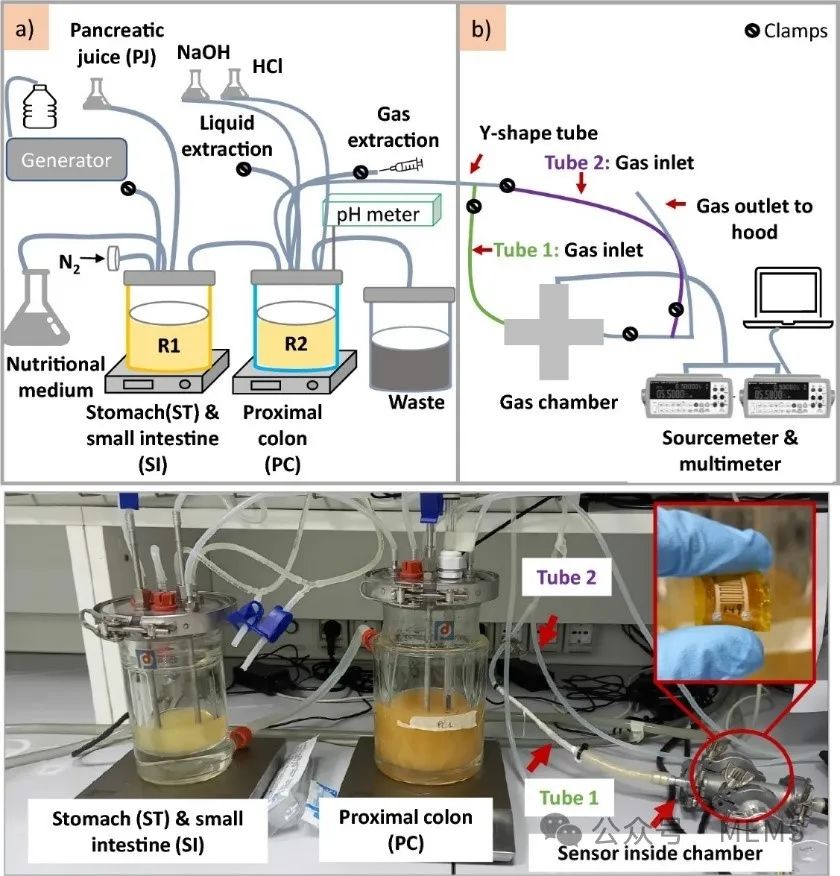
电池装置为传统双室构型,材质为有机玻璃,阴阳两室有效体积均为118mL,中间隔以阳离子交换膜(CMI7000)。使用预处理后的碳毡(30mm×30mm×2mm)作为电极材料,阴阳电极用钛丝(直径为0.6mm)连接并用橡胶塞固定,两电极以3cm间隔平行相对。用氮气吹扫两极室保持厌氧环境,外接1000Ω电阻构成闭合回路。双室MFC运行温度为(30±2)℃。
电能采集装置包括数据采集器与电脑两部分。数据采集器为蓝博电池测试系统(LANBNTS,BT-2018C),通过与电脑连接实时显示电能数据并记录。参数设置:电压范围0~5V,采集精度1mV,采集频率5min/次。
活性污泥取自上海市某污水处理厂二沉池,用蒸馏水淘洗3遍,并经200目筛网过滤杂质,随后加入适量阳极液,厌氧条件下置于磁力搅拌器室温下搅拌3~5d,静置分层去上清液,密封备用。本实验双室MFC系统均添加厌氧污泥,厌氧污泥与阳极室的体积比为1∶4。
S.oneidensisMR-1菌液培养:无菌条件下,用接种环挑取活化后的S.oneidensisMR-1单菌落,接入灭菌冷却后的LB培养基中,在30℃、120r/min条件下培养至对数生长末期。LB液体培养基由10g/L胰蛋白胨、5g/L酵母提取物和10g/LNaCl组成。
实验涉及的3组MFC系统包括不添加产电菌的双室MFC、游离态细胞双室MFC和固定化细胞双室MFC,依次标记为MFC1、MFC2和MFC3。
本实验选用的阴阳电极材料均为碳毡,使用之前需经酸性重铬酸钾浸泡(60℃水浴加热30min)与马弗炉预处理(450℃加热30min),预处理后的碳毡可直接作为电极。其中,MFC3的碳毡阳极需进一步处理,制备方法为将预处理后的碳毡连接钛丝,与3mLS.oneidensisMR-1液体菌液共同加入灭菌后的LB培养基,在35℃、120r/min条件下培养7d。MFC2加入产电菌的方式为向阳极室添加S.oneidensisMR-1菌悬液5mL。MFC1的接种物仅为厌氧污泥。通过调整OD600将3组MFC装置的阳极液生物量保持一致。3组MFC装置的阴极液均为0.1mol/L铁氰化钾溶液,为保证充足的电子受体,当阴极液由黄色变为浅绿色时更换阴极液。
在启动阶段,将阳极液加入MFC阳极室,阳极室初始COD在(2000±100)mg/L,连续两个周期最大电压相近视为启动成功。在正式运行阶段,将阳极液更换为模拟制药废水,电压降至50mV以下视为一个周期结束,需更换阴阳电极液持续运行,每周期阳极初始COD保持在(3000±100)mg/L,连续运行3个周期。
电化学性能:电压U通过电能采集装置采集;电流I根据式(1)欧姆定律计算;电流密度IA根据式(2)计算;功率密度(PA)根据式(3)计算;极化曲线与功率密度由外电阻法测定,外接电阻箱由高到低改变电阻值,依次为10000、8000、6000、4000、2000、1000、800、600、400、200、100Ω,每个阻值下运行15~20min并记录;电池内阻r由极化曲线斜率求得;阳极生物膜的循环伏安曲线(CV)通过三电极体系测得,扫描速度为10mV/s,扫描电压为-0.8~0.4V,其中对电极为铂丝电极,参比电极为Ag/AgCl电极,工作电极为阳极碳毡。

式中:I——电流,mA;U——电压,mV;R——电阻,Ω;IA——电流密度,mA/m2;A——阳极面积,m2;PA——功率密度,mW/m2。
苯酚采用四氨基安替比林法测定;COD与NH4+-N根据国标法测定;库仑效率(CE)根据式(4)计算。

式中:CE——库仑效率;M——O2的摩尔质量,32g/mol;t——周期运行时间,s;I——t时刻的电流,mA;V——阳极室体积,mL;F——法拉第常数,96485C/mol;ΔCOD——运行始末的COD变化量,g/L。
阳极碳毡经戊二醇溶液固定、磷酸盐缓冲液冲洗、梯度乙醇溶液脱水、冷冻干燥、喷金处理后,使用扫描电子显微镜(ZEISSGeminiSEM300)观测阳极生物膜形貌。
运行结束后,将阳极碳毡放入PBS无菌缓冲液中摇床振荡30~60min,将阳极碳毡取出,先用两层无菌纱布过滤去除杂质,再用0.22m硝酸纤维素滤膜过滤,将滤膜送检16SrRNA测序。
各MFC系统的启动电压、正式运行输出电压、极化曲线与功率密度、CV曲线。

各MFC系统启动过程分为两个阶段,各阶段电压变化如图2(a)所示。在第Ⅰ阶段,MFC1、MFC2、MFC3达到最大电压所需时间分别为108、93、82h,对应的最大电压分别为325、452、517mV。为进一步在阳极上富集优势产电菌群及提升各装置产电性能,在电压下降阶段向各装置阳极分别加入1g葡萄糖以补充碳源。在第Ⅱ阶段,电压迅速上升,MFC1、MFC2、MFC3的最大电压分别升高至402、528、618mV,且最大电压持续时间明显增加,视为各MFC系统启动成功。待电压降至100mV以下,将阳极液更换为模拟制药废水持续运行3周期。
在正式运行阶段,各实验组输出电压随时间变化过程如图2(b)所示。可观察到,由于3组装置的阳极中首次加入制药废水,3组MFC装置处于适应阶段,在第Ⅰ周期MFC1、MFC2、MFC3的最大输出电压均低于启动过程的第Ⅱ阶段,分别为351、512、572mV。在第Ⅱ、Ⅲ周期,随阳极表面生物膜逐渐成熟,微生物传递到阳极的电子数量增加,系统趋于稳定,各实验组最高输出电压持续增加,均在第Ⅲ周期取得最大电压,且在较高电压下持续时间增长,MFC1、MFC2、MFC3输出电压分别为384、535、633mV。由此可以看出,在本研究制备的3组MFC装置中,以制药废水为阳极液用于发电是可行的。
在第Ⅲ周期测得各装置极化曲线与功率密度曲线(c)所示。MFC1、MFC2、MFC3的最大功率密度分别为280.9、477.9、582.7mW/m2,内阻分别为516.7、459.2、398.8Ω,开路电压分别为674、808、836mV。另外,可观察到在改变外电阻过程中,当外接电阻由万欧、千欧级降低到百欧级时,由于阳极微生物对底物的利用存在阻力以及电子传递过程存在阻力,微生物无法提供足够的电子以供产电,导致产电量迅速减少,功率密度曲线与极化曲线中出现回折。为进一步探究阳极生物膜的电活性,对比分析各实验组碳毡阳极的循环伏安曲线(
CV),如图2(d)所示。相比MFC1,MFC2、MFC3阳极生物膜的氧化还原峰较明显,峰值电流分别为3.2、3.7mA。其中,MFC3的峰值电流最高,CV曲线积分面积最大且对称性较好,说明固定细胞MFC阳极生物膜活性较高,电子转移效果及对称性更佳。上述结果表明,添加产电菌的两组
MFC的产电性能较仅添加污泥的双室MFC产电性能明显提升,且启动时间缩短,MFC3产电性能最佳,其最大功率密度较MFC1、MFC2分别提高了107.4%、21.9%。在阳极室中添加产电菌S.oneidensisMR-1提升了MFC的产电性能,其促进系统产电的原理为S.oneidensisMR-1内膜、外膜和周质空间存在的多种氧化还原蛋白能通过直接和间接电子传递过程进行有氧/无氧呼吸,并分泌核黄素作为参与胞外电子转移过程的氧化还原介体,提升胞外电子转移能力,促进阳极氧化反应,进而提升系统的氧化还原反应速率。2.2
MFC系统阳极室污染物降解效果及间接掌握微生物菌群的代谢情况,在正式启动后对3组MFC装置阳极室COD、NH4+-N、苯酚、库仑效率进行3周期监测,各周期污染物去除率见表1,3周期内污染物平均去除效果及各周期库仑效率见图3。


3(b)可见,3周期内MFC1、MFC2、MFC3的平均NH4+-N去除率相差不大,分别为70.0%、72.7%、74.1%,NH4+-N能否在生物电化学系统中直接作为电子受体尚无定论,阳极室的NH4+-N主要通过厌氧氨氧化作用、厌氧反硝化作用、氨氮迁移作用去除。由图
3(c)可见,3周期内MFC1的平均苯酚去除率最低,为74.6%,而MFC2和MFC3的平均苯酚去除率相近,分别为80.5%、82.0%。通过MFC降解含苯酚废水是可行的,相关研究表明与单一苯酚燃料相比,以苯酚和葡萄糖混合物为燃料更易促进MFC系统的产电性能。库仑效率(
CE)能够反映各周期底物基质转移到阳极的实际电子数量与理论电子数量之间的关系,是评价MFC对废水处理效果的重要指标之一。由图3(d)和表1可见,MFC1的库仑效率先升高后下降,而MFC2与MFC3的库仑效率在第Ⅱ、Ⅲ周期内均升高,MFC1、MFC2、MFC3在3周期内的平均库仑效率分别为16.3%、23.2%、26.6%。MFC2、MFC3的底物有效产电利用率较高,产电菌S.oneidensisMR-1对MFC系统起到了生物强化作用,加强了系统产电性能与污染物去除能力。在第

MFC1,MFC2和MFC3的各污染物去除速率均有明显提升,MFC3的各污染物去除速率最高。经一级反应动力学拟合,MFC3去除COD、NH4+-N、苯酚的一级反应动力学速率常数分别为0.18(R2=0.99)、0.13(R2=0.97)、0.16d-(1R2=0.98)。通过对比污染物去除率与去除速率得出,固定化细胞
MFC对污染物去除效果最佳。ZhuangzhuangLIU等从猪粪中分离出1株新型四环素脱除菌,该菌株在游离态对四环素最高去除率为71.62%,使用羧甲基纤维素和聚多巴胺固定活细胞后,四环素去除率达到91.16%。游离态菌株易与原有菌群竞争,导致存活率较低,影响污染物去除效果,而固定化细胞技术能有效提高细胞密度及活性,更适用于降解复杂污染物。在本实验3周期的测试中,固定化细胞MFC的产电性能与污染物去除能力最佳,与其他熊猫体育智能股份相关研究(表2)对比,固定化细胞技术应用于MFC系统中具有在去除复杂污染物同时产生电能的潜力。


5(a)为仅经重铬酸钾溶液与马弗炉加热预处理的空白碳毡,其表面光滑、缝隙大,为微生物的附着提供了条件。随MFC成功启动与运行,微生物在阳极表面富集成膜,图5(b)、图5(c)和图5(d)分别为MFC1、MFC2和MFC3的阳极形貌图,MFC2、MFC3的阳极比表面积与粗糙度较大,有利于微生物的附着,附着微生物的种类更为丰富。2.4
阳极生物膜微生物群落结构分析阳极生物膜菌群结构是影响污染物去除和电能产生的重要因素,阳极微生物群落之间存在协同作用,具有不同功能的微生物(如产电菌、水解细菌与发酵细菌)在系统中共存,降解污染物并获得电能。阳极生物膜在门水平和属水平下的微生物结构组成见图

6可知,与不添加产电菌的MFC1相比,添加游离态细胞的MFC2、固定化细胞的MFC3的阳极生物膜细菌群落结构发生了一定变化。在门水平下,3组装置阳极生物膜的前4种优势菌门均包括Proteobacteria(变形菌门)、Bacteroidota(拟杆菌门)、Desulfobacterota(脱硫杆菌门)和Firmicutes(厚壁菌门),是常见于MFC系统的电活性菌门,可进行厌氧消化并增强系统产电性能,这4种优势菌门在MFC1、MFC2、MFC3中的总相对丰度分别为69.63%、78.13%、83.23%,且各MFC系统4种优势菌门构成比例有所不同。在属水平下,变形菌门中典型的电活性微生物
)将产电菌S.oneidensisMR-1以游离态与固定化形式加入双室MFC同步处理模拟苯酚制药废水,S.oneidensisMR-1加快了电子传递与氧化还原反应速率,提升了对污染物的处理效果与发电性能,对MFC系统起到了生物强化作用,为废水中污染物的去除和能源转化提供了新思路。2
)固定化细胞双室MFC产电性能与污染物去除效果均优于游离态细胞双室MFC。在3周期的连续运行下,固定化细胞双室MFC系统的最大输出电压、最大功率密度、平均COD去除率、平均库仑效率分别为633mV、582.7mW/m2、82.熊猫体育智能股份5%、26.6%,与游离态细胞双室MFC相比分别提升了18.7%、21.9%、10.9%、14.7%,固定化细胞技术具有在MFC中实际应用的潜力。3